Wow! Taiwan Project
財團法人商業發展研究院行銷與新媒體研究所於 2019 年開展 Wow! Taiwan Project。
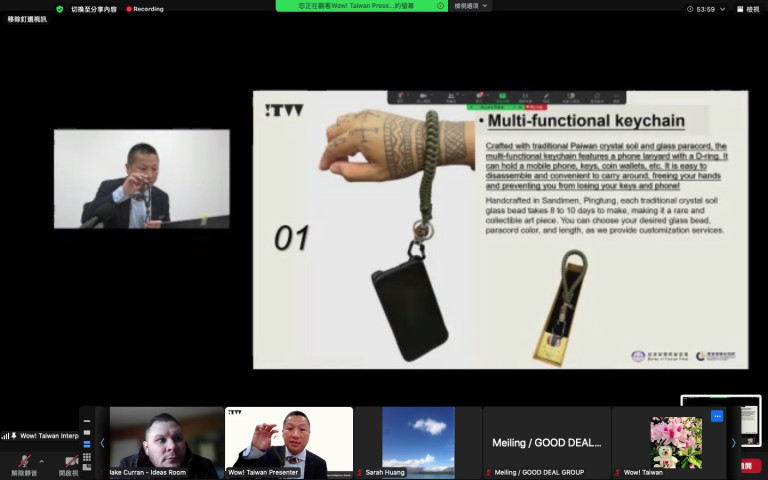
「Wow! Taiwan Project」是執行海外拓銷的D2B (Direct to Buyer) 數位策展平臺,推廣臺灣優勢產業解決方案;並邀請國際買家成為長期合作夥伴,舉辦線上媒合會,以協助臺灣中小企業與國際買家建立直接媒合渠道。
現在,我們邀請全球買家註冊為我們的合作夥伴,並在線上媒合會中與我們的品牌代表進行商務洽談。
貿易沙龍
最新公告
註冊會員,隨時掌握新南向市場情報
2024
03/11
113年度新南向市場創新行銷計畫 熱烈報名中(台北場YouTube同步直播影片)
受理申請截止時間:自公告日起至113年4月2日(二)止
02/15
113年度新南向市場創新行銷計畫年度拓銷說明會-台北場
2024.03.07 集思北科大會議中心 感恩聽(台北市大安區忠孝東路三段1號 億光大樓2樓)
02/15
113年度新南向市場創新行銷計畫年度拓銷說明會-高雄場
2024.02.29 高雄軟體育成中心 開創會議室(高雄市前鎮區復興四路2號4樓)
02/15
113年度新南向市場創新行銷計畫年度拓銷說明會-台中場
2024.02.22 集思台中文心會議中心 G3會議室(台中市西屯區文心路二段107號4樓)
01/23
113年新南向市場創新行銷計畫-年度拓銷專案受理公告
受理申請截止時間:自公告日起至113年4月2日(二)止